

一、医疗器械监管机构
墨西哥联邦卫生风险保护委员会COFEPRIS (Comisión Federal para la Protección contra Riesgos Sanitarios),是墨西哥的卫生监管机构,负责药品、化妆品、食品、医疗器械和其他相关产品的注册、监管和监督事务。
二、主要法规
Ley General de Salud (LGS)
(《一般卫生法》》)
Ley Federal de Procedimiento Administrativo (LFPA)
(《联邦行政程序法》)
Reglamento de la Ley General de Salud en Materia de investigación para la salud
(《一般卫生法关于健康研究的规定》)
Reglamento de Insumos para la Salud (RIS)
(《卫生用品条例》)
三、医疗器械市场准入的注册流程
COFEPRIS注册的前提条件:
所有在墨西哥销售的医疗器械都需要在墨西哥联邦卫生风险保护委员会COFEPRIS进行注册并获得相应的注册证书。
在墨西哥销售医疗器械的外国制造商需要指定一个注册信息持有人(Mexico Registration Holder), 即墨西哥当地代表,向墨西哥卫生当局进行技术资料或者相关文件的提交,负责注册相关事宜。
1.医疗器械注册流程概述
→确定产品分类
→指定墨西哥当地授权代表
→准备技术文档,提交申请
→审核通过,申请人获取注册证书
2.医疗器械注册流程详述
A.标准审查路径:
①确定产品分类
Reglamento de Insumos para la Salud (RIS) ,ARTÍCULO 83
(《卫生用品条例》第83条)
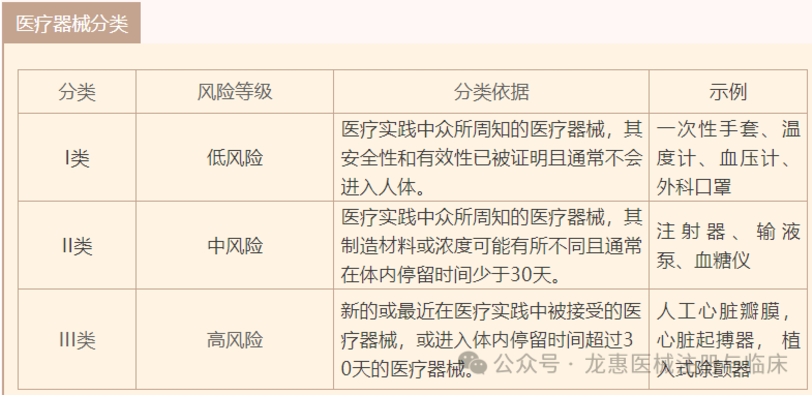
医疗器械根据其风险等级被分为三个类别: I类、II类和III类
* Diario Oficial de la Federación联邦官方公报协议清单所列产品,如运动和康复用脚踏板等,无需进行登记注册。
②注册材料准备
Reglamento de Insumos para la Salud (RIS).
(《卫生用品条例》)
GUIA PARA LA OBTENCION DEL REGISTRO SANTRARIO DE DISPOSITIVOS MEDICOS CLASE I,II Y III
(《医疗器械I、II和III类注册要求指南》)
I类、II类、III类:
(1)使用说明书或操作手册
(2)证明产品满足安全性和有效性特征的技术文件
(3)符合标准的标签
(4)生产工艺描述
(5)医疗设备的结构、材料、部件和功能的说明
(6)检测报告
(7)原产国卫生主管部门出具的自由销售证书或同等证明
(8)如果产品不是由墨西哥申请注册的母公司/工厂/实验室生产的,则应提供制造商的声明函;
(9)原产国卫生主管部门颁发的GMP证书/ISO 13485证书/等效证书
(10)产品制造商出具的分析证书(certificate of analysis)原件
(11)其他文件如有要求
* 西班牙语提供
关于标签和使用说明书:
标签,应注意:
(1)可重复使用的无菌医疗器械必须在使用说明书或标签/标签样稿中注明用于重复灭菌的方法
(2)无菌产品的具体图例
(3)说明产品为一次性或不可重复使用(如适用)。
(4)标签样稿以文本和Word文件的形式提供。应包括提交清单,以及每个医疗器械提交的描述和代码或目录号(如适用);它们必须与所提交的自由销售证书和技术/商业文件中注明的内容相对应
说明书,应包含以下信息:
(1)通用名称
(2)产品描述
(3)预期用途
(4)产品展示
(5)组件或部件列表(如适用)
(6)可组装和可拆卸性(如适用)
(7)操作、清洁和灭菌(如适用)
(8)贮存条件(如适用)
(9)维护(如适用)
(10)校准(如适用)
(11)注意事项
(12)准备工作(如适用)
(13)警告(如适用)
(14)禁忌症(如适用)
(15)不良事件(如适用)
(16)对于配制产品,应包括给药途径、剂型和活性成分含量(如适用)
(17)外科技术相关信息(如适用)
*西班牙语提供
B.等效性审查路径:
已经获得美国食品和药品监督管理局(FDA)批准、加拿大卫生部(HC)或日本厚生劳动省(MHLW)批准,符合条件的医疗器械和技术,则可能有资格获得等效性审查。等效性审核要求提交一份摘要性的资料,但是对于技术信息的要求没有那么详细。
C.第三方审查路径:
除以上的标准审查路径和等效性审查路径以外,墨西哥注册还有另外一种路径,即第三方审查(TPR)。
第三方审查人是由COFEPRIS授权对医疗器械申请进行“预批准”的独立、经认可的商业实体。它们是墨西哥本地公司,与任何全球公认的注册商/认证机构都没有关联。他们将详细审查档案,通常会在签发预批准函之前要求制造商提供更多信息。然后,COFEPRIS将完成最终审查并颁发注册证书。使用TPR需要收费。

