医疗器械可用性工程,又叫做人因工程,是指通过研究设备的使用对象、用户的任务、使用环境,将人类的行为、能力、限制以及其他特点的知识应用到医疗器械的设计之中的过程,目的是设计出优秀的用户界面,将设备的使用相关风险降到可接受的水平,让用户在预期的使用场景之下,安全并有效地使用医疗器械。
用户界面:用户界面/用户接口(User Interface)不仅仅是设备的屏幕和按钮。在谈到医疗设备时,各种随附文档以及用户可以与之交互的几乎所有内容都需要被视为用户界面。产品说明书、设备标签、设备报警的视觉和听觉信号等都属于用户界面的构成部分。
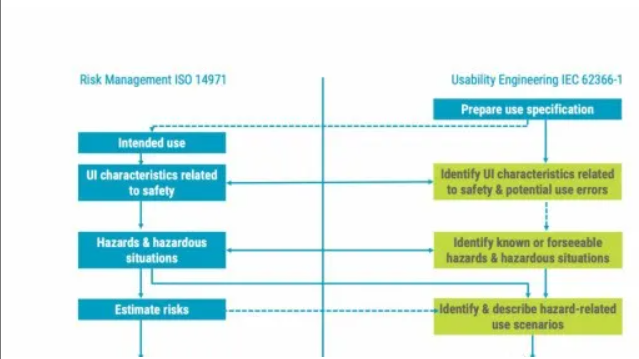
根据IEC62366-1和FDA发布的《医疗器械应用人因与可用性工程指南》,医疗器械可用性基本流程可大致分为以下几个环节: 1. 撰写使用说明 2. 分析设备和用户界面的安全性 3. 识别与危险相关的使用场景 4. 归纳用户界面要求 5. 完善设计&形成性评估 6. 总结性评估 01撰写使用说明 可用性工程应从编写使用说明 (Use Specification) 开始。这是一份包含有关设备用户所有信息的文件。它可以看作是设备预期用途的扩展形式,包括对设备预期用户的用户研究和设备使用环境的观察。 不同的用户和使用环境会产生不同的使用风险。我们以血糖测量设备为例。如果该设备在家庭环境中供幼儿、老年人使用,那么与在医院环境中供专业护理人员使用的设备相比,设备使用的潜在风险水平和风险发生的形式都会有所不同。 为了确保设备使用的安全性和有效性,确定环境中正确的设备与用户配置,并记录下用户所有的特征信息是非常重要的。这不仅需要记录归纳预期用户的人体特征和人群属性,还包括在设备操作和使用环境中可能引发潜在使用相关风险的所有特性。 02分析设备和用户界面的安全性 在了解使用环境和用户特点的基础上,进一步分析设备在安全性和用户界面方面可能出现的问题。这就类似于根据 ISO 14971 标准去识别风险或回应与设备安全有关的问题,某种程度上,我们可以把可用性工程看作是风险管理流程的工具/一部分。 安全性在医疗设备的可用性工程中扮演着重要角色。“使用错误”是一个常见的术语。 使用错误:用户在使用医疗设备时的一个行为,或缺少了某个行为--导致与制造商预期或用户预期不同的结果"。——IEC 62366-1 使用错误的这一定义非常广泛。可以说,每次人类和机器 "误解 "对方时,都会发生使用错误。使用错误的典型例子可能是护士在没有注意到的情况下不小心拔出了监护设备传感器的电缆,又或者是医护人员在将无菌纸巾敷于伤口前用手指触摸了无菌纸巾。当制造商意识到上述情况下可能存在设备突然断电、细菌感染等不可接受的危害时,就需要考虑设备的用户界面该如何预防/应对这些因使用错误引发的风险。 但并不是每一次使用错误都会导致危险情况的发生。可用性工程所关注的是会导致高风险(危害大/发生频次高)的使用错误。