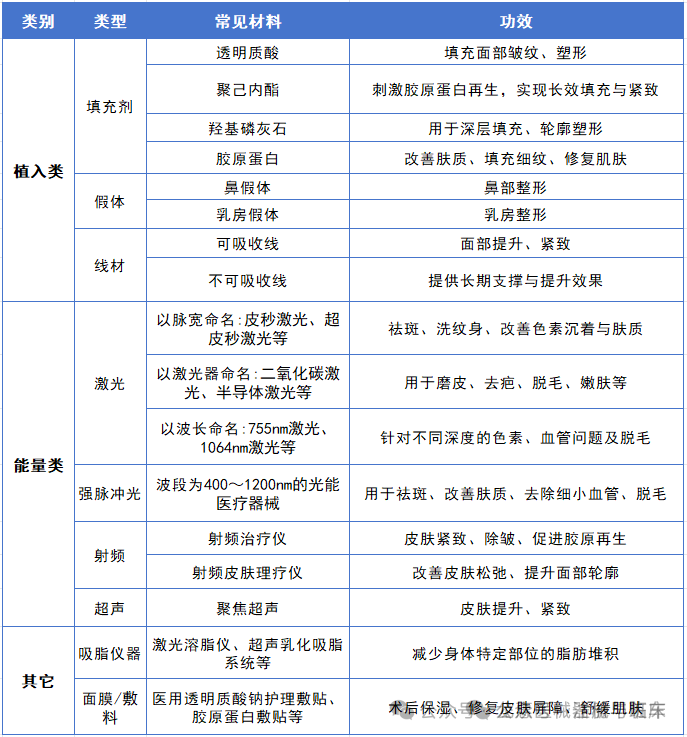
近年来,我国“悦己消费”不断升级,医美市场持续高速发展。伴随行业扩张,医美类医疗器械不仅迎来更多创新机遇,也面临着日益严格的监管要求。在此背景下,构建科学、规范的生物学评价体系,成为提升产品安全性、推动行业健康有序发展的关键。
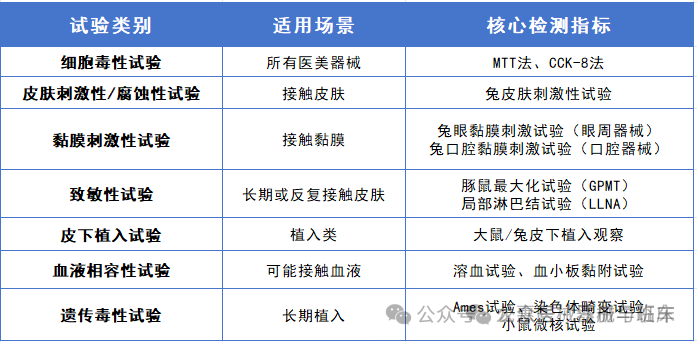
医美类医疗器械分类 医疗器械生物学评价路径 医美类医疗器械种类繁多,不同产品的理化特性和临床使用场景差异较大,通过科学规范的生物学评价,可以全面评估医美类医疗器械与人体接触时可能产生的各种生物学反应,包括细胞毒性、致敏性、刺激性等,从而确保将医美类医疗器械在使用过程中对人体造成危害降到最低。目前,从实际操作情况来看终点评价的路径应用范围较广。 1.等同性分析 从材料配方、加工工艺和灭菌方式、几何和物理特性以及人体接触方式和临床使用途径等方面与已上市的可比器械进行比较,根据GB/T 16886.18标准证明材料等同和终点等同。 适用于同一家企业在产品迭代过程中与已上市可比器械进行等同性分析,可豁免全部生物相容性试验。 2.毒理学分析 从临床前数据、临床数据和试验数据中获得毒理学资料,结合合理的化学表征进行毒理学分析。 适用于有足够且合理毒理学资料的医疗器械,对试验人员的毒理学背景要求极高,在某些情况下可豁免部分生物相容性试验。 3.终点评价 通过识别数据缺口,选择评价终点,补充生物相容性试验或临床前大动物试验完成生物学评价。 适用于无法通过等同性分析和毒理学分析完成生物学评价的医疗器械。 常规生物相容性试验 动物有效性试验 在“替代、减少、优化”伦理原则框架下,动物试验是医美医疗器械研发注册中不可或缺的环节,是连接体外试验与人体临床试验的关键桥梁,为产品的安全性与有效性提供了全面且可靠的科学支撑: 安全前置筛查:避免直接人体试验的风险,提前发现材料植入/作用后的炎症、排异、降解毒性等问题。 模拟真实效果:在接近人体的生理环境中,验证填充持久性、胶原再生、能量器械的组织响应等核心医美效果。 优化操作参数:通过动物模型调试激光能量、填充剂量等关键参数,确定安全有效的使用范围。