

据国家药监局于2024年7月发布的《国家药监局关于进一步明确射频治疗仪类产品有关要求的公告(2024年第84号)》显示,自2026年4月1日起,《关于调整〈医疗器械分类目录〉部分内容的公告》(2022年第30号,以下简称30号公告)附件中09-07-02射频治疗(非消融)设备中射频治疗仪、射频皮肤治疗仪类产品,未依法取得医疗器械注册证的,不得生产、进口和销售。
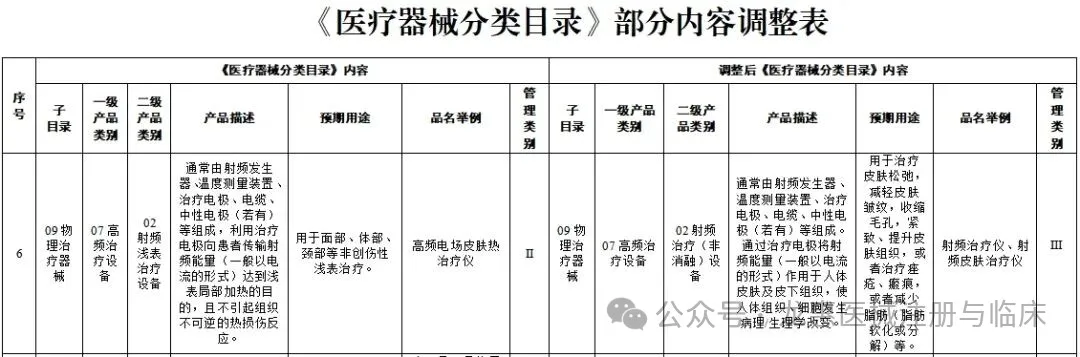
已取得第二类医疗器械注册证的,原注册证在有效期内继续有效。原注册证在2026年4月1日前到期的,注册人可向原审批部门提出原注册证延期申请,延长期限最长不得超过2026年3月31日。
哪些射频类产品属于医疗器械
国家药监局器械标管中心曾于2024年3月发布《射频治疗仪、射频皮肤治疗仪类产品分类界定解读》。其中对涉及美容用途射频类产品的管理属性和管理类别划分进行了明确。
1、并非所有射频类产品都属于医疗器械;
2、根据30号公告,按照医疗器械管理的射频治疗仪、射频皮肤治疗仪类产品,其工作原理一般是“通过治疗电极将射频能量作用于人体皮肤及皮下组织,使人体组织、细胞发生病理/生理学改变”;预期“用于治疗皮肤松弛,减轻皮肤皱纹,收缩毛孔,紧致、提升皮肤组织,或者治疗痤疮、瘢痕,或者减少脂肪(脂肪软化或分解)等”。符合30号公告规定的产品应当作为第三类医疗器械管理。
3、不符合医疗器械定义的射频类产品,则不作为医疗器械管理。
