

上海市医疗器械化妆品审评核查中心对2025年本市进口转产体外诊断产品(涵盖体外诊断试剂及配套使用设备)注册体系现场核查情况开展分析发现,不符合项主要集中于设计开发、采购管理、生产管理与质量控制四个环节。本期围绕上述高频不符合项进行梳理分析,帮助企业精准识别质量管理体系薄弱环节,加强体系合规管理,保障转产工作平稳高效推进。
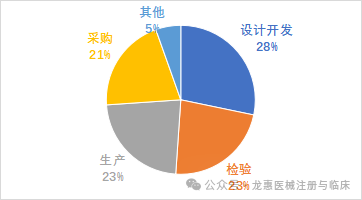
图 进口转国产医疗器械注册现场核查不符合项分布(体外诊断产品)
设计开发作为体外诊断产品质量保证的核心环节,其技术转移过程直接决定了转产产品能否实现从进口到国产的实质性转化。《医疗器械生产质量管理规范(2014年第64号)》(以下简称现行《规范》)中明确要求:在进行设计和开发策划时,应当确定设计和开发的阶段及对各阶段的评审、验证、确认和设计转换等活动,应当识别和确定各个部门设计和开发的活动和接口,明确职责和分工。
高频不符合项1
未能提供与境外企业签订的明确的设计开发转移协议,申报产品技术转移资料不完整。
问题示例1
现场查见转产企业与境外企业签订的转移协议仅为框架协议,未明确转移资料的具体内容,部分设计和开发输出文件不完整,如未包含反应体系研究、零部件图纸、软件核心算法说明书等输出文件。不符合现行《规范》现场检查指导原则*5.4.1
器审小编提示
现行《规范》现场检查指导原则中*5.4.1条明确设计和开发输出应当满足输入要求,设计和开发输出资料至少符合以下要求:“2.生产和服务所需的信息,如产品图纸(包括零部件图纸)、工艺配方、作业指导书、环境要求等;7.提交给注册审评部门的文件,如研究资料、产品技术要求、注册检验报告、临床评价资料(如有)、医疗器械安全有效基本要求清单等”。针对转产产品,国家药品监督管理局发布《关于进一步调整和优化进口医疗器械产品在中国境内企业生产有关事项的公告》(2025年第30号,以下简称《公告》)中明确:对境内注册申请人开展核查,同时重点关注产品设计开发环节境内外质量管理体系的实质等同性。转产企业通过与境外企业签订设计开发转移协议,将境外企业的技术资料转移至境内,协议需明确产品转移范畴及具体内容,从而确保产品的设计开发资料的完整性与一致性。
规范建议
建议转产企业在项目立项阶段,可对照产品注册申报资料要求(可参考国家药品监督管理局2021年第121、122号公告),依据产品特性梳理并建立技术文件输入清单,与境外企业签订转移协议时,可以附件的形式明确上述技术文件交付清单。必要时,可建立技术文件接收清单,梳理并确认转移的完整性。试剂类产品需包含主要原材料、反应体系、生产工艺文件等输出资料。设备产品需包含总装图及部件图、软件开发文档、软件功能测试报告、核心算法等内容。
高频不符合项2
技术资料由境外企业转移而来,工艺文件未进行本地转化。
问题示例2
现场查见的生产作业指导书由境外企业转移的技术文件翻译而来,未考虑生产条件(如反应釜容量、投料量)的变化可能产生的差异性,转产企业未对参数的适用性进行评价。不符合现行《规范》现场检查指导原则5.5.1
器审小编提示
现行《规范》现场检查指导原则中5.5.1条中已明确:应当在设计和开发过程中开展设计和开发到生产的转换活动,以解决可生产性、部件及材料的可获得性、所需的生产设备、操作人员的培训等。生产作业指导书作为设计和开发输出资料,应当在成为最终产品规范前得以验证,确保设计开发输出的生产环境、原材料控制、生产工艺和质量控制等相关规程得到验证并适用于商业化生产。
规范建议
对于已获进口医疗器械注册证的产品,生产工艺文件可通过转移的方式转至境内转产企业,仍需结合现行《规范》的要求根据产品特性开展设计开发到生产的转换活动,对转移文件如工艺文件进行本地化转换,建议充分考虑法规、环境设施、人员等差异,对关键工艺参数完成验证、确认、转化、变更及评审等活动及输出要求,确保其适用于生产,从而保证产品的性能指标与已获证进口医疗器械保持一致。
高频不符合项3
部分辅料采用国产化替代,但企业未充分评估可能带来的产品风险。
问题示例3
现场查见产品组成中的抗生素(非主要组成成分)生产商由进口变更为国产,企业未充分评估该成分变化可能导致的产品风险。不符合现行《规范》现场检查指导原则中*5.10.3
器审小编提示
现行《规范》现场检查指导原则*5.10.3条中已明确:当选用的材料、零件或者产品功能的改变可能影响到医疗器械产品安全性、有效性时,应当评价因改动可能带来的风险,必要时采取措施将风险降低到可接受水平,同时应当符合相关法规的要求。体外诊断试剂附录中也规定研究过程中涉及的主要原材料、中间体、重要辅料等应当明确来源并符合要求。
规范建议
在转产过程中,如选用的非关键原材料或零部件发生变更,需开展相关评审,做好风险评估,必要时开展验证或确认活动。体外诊断试剂类产品的评估建议包括产品技术要求中的各性能指标以及稳定性指标;设备类产品建议纳入电气安全指标。
器审小编提示
上述规范建议已对标《医疗器械生产质量规范(2025年第107号)》修订内容,核心要求基本一致,可为企业新旧法规衔接、产品合规落地提供参考。
