

Q:什么是采用脑机接口技术的医疗器械?
参考YY/T 1987-2025《采用脑机接口技术的医疗器械 术语》中的定义,指通过侵入或非侵入的方式,测量中枢神经系统产生的神经信号并实时解码,实现患者与外部辅助或诊疗设备的实时双向交互或闭环反馈,达到改善、修复或替代中枢神经系统功能等临床效果的有源医疗器械。通常包括侵入式脑机接口医疗器械和非侵入式脑机接口医疗器械。
Q:《申报产品有适用的指导原则》,但修订版目前处于征求意见中,如何执行该指导原则?
应执行现行有效的指导原则。修订版指导原则待国家药品监督管理局发布后即实施。
Q:按照第二类医疗器械管理的注射泵/输液泵的适用范围应如何规范?
适用范围应按照《医疗器械分类目录》中14-01-01和14-02-01的要求明确“不用于镇痛药、化疗药物、胰岛素的输注。”。用于对镇痛药、化疗药物、胰岛素进行输注的该类产品按第三类医疗器械管理。
Q:关键元器件改变,需要重新检测、变更注册吗?
企业需自行评估该元器件变化是否影响产品安全有效性(比如元器件参数是否变化),一般应采取检验等方式进行合理评估;如不涉及产品注册证及其附件载明信息变化,可不进行变更注册。
Q:我司欲申报II类医疗器械软件,对比产品可以选择有源器械的上位机软件组件做对比吗?
需结合具体情形确定可行性。只有在同时满足 “同预期用途、同核心功能” 的有源器械上位机软件组件,可以作为对比产品;否则不能作为对比产品。另外,咨询问题过于笼统,在实际工作中,还需要进一步识别具体路径如:(1)免于临床评价;(2)同品种临床评价。在实际工作中,这两个途径的具体要求和规则也不相同。
Q:元器件改变,需要评估该元器件变化是否影响产品安全有效性(比如元器件参数是否变化),如元器件参数变化,一般应采取检验等方式进行合理评估,需要评估安规和电磁兼容吗?电磁兼容一般企业没有自检能力,需要找三方检测机构去检测吗?
自行评价变化影响决定是否需要检验验证。
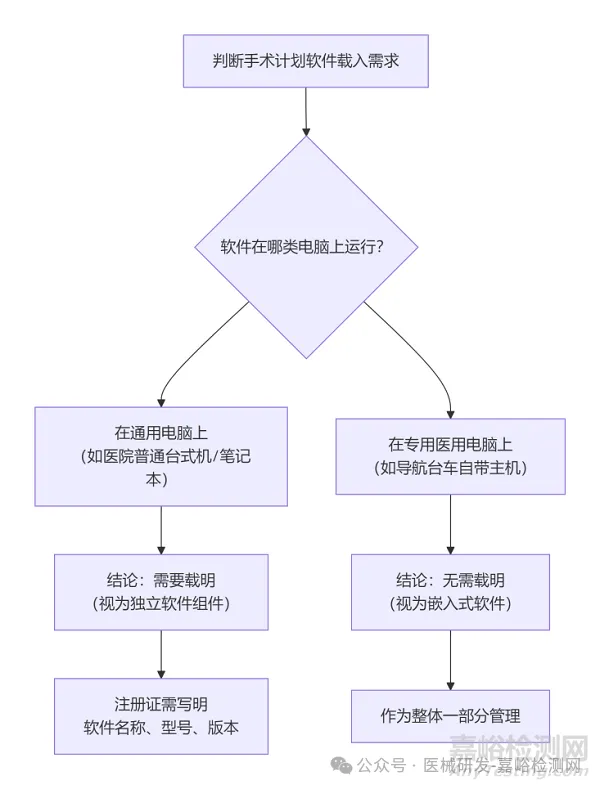
Q:产品结构组成中是否需要载明其包含的手术计划软件?
对于包含手术计划软件的产品,其软件组件信息是否需要载明于医疗器械注册证的“结构及组成”中,取决于其类型和功能定位。
①核心判断标准
如果该手术计划软件单独运行于通用计算平台(例如通用的台式计算机、笔记本电脑),则应视为独立软件形式的软件组件,必须在注册证中明确载明其软件组件名称、型号和发布版本。
反之,如果软件并非以上述方式独立运行,则通常无需在注册证的结构组成中单独列出。
即:
软件运行特征 | 是否需在注册证结构组成中载明 |
手术计划软件单独运行于通用计算平台(如通用电脑) | 是,需载明软件组件名称、型号、发布版本 |
软件属于嵌入式组件,或运行于设备专用的医用计算平台(如导航台车自带计算机) | 否 |
②需要载明的具体要求
根据《医疗器械软件注册审查指导原则(2022年修订版)》及相关规范要求,对于作为软件组件管理的软件,在产品技术要求中需包含以下核心信息:
软件标识信息:必须明确软件的名称与型号规格,确保与注册申报信息完全一致。
版本信息:必须注明软件版本号。版本号的命名规则应能体现重大更新(如主版本号变更通常涉及安全性或功能性重大升级),并包含主版本号、次版本号和补丁号,提供完整的发布版本。
产品技术要求中的体现:对于含有软件组件的医疗器械,在产品技术要求第一部分应描述软件名称、发布版本号、完整版本号;在第二部分需明确软件的全部临床功能纲要。
③作为嵌入式组件的管理
当手术计划软件作为嵌入式软件,运行于设备专用的医用设备(如导航台车的计算机)时,它被视为医疗器械整体功能的一部分。在这种情况下,虽然不需要在注册证结构组成中单独列出该软件,但其安全性与有效性的管理要求并未降低。
软件仍需按照《医疗器械软件注册审查指导原则》进行全面的验证与确认,相关研究资料需在注册申报时提交。
由于具体产品的设计可能存在特殊情况,在最终确定申报策略前,建议通过官方渠道与相应的药品监督管理部门进行事前沟通咨询,以获取最准确的指导。
